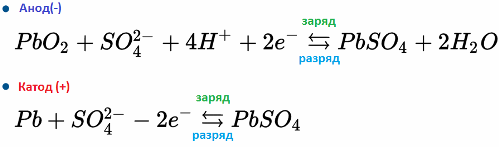Категорије: Како то ради?, Ауто електричар
Број прегледа: 16526
Коментари на чланак: 0
Уређај и принцип рада батерије
Позвана је електрична батерија хемијски извор струје за вишекратну употребу. Хемијски процеси унутар батерије, за разлику од оних у једнократним галванским ћелијама, попут алкалних или сланих батерија, су реверзибилни. Циклуси наелектрисања, накупљања и повратка електричне енергије могу се поновити више пута.
Дакле, принцип рада батерије омогућава вам да је циклично користите за аутономно напајање разних уређаја, преносних уређаја, возила, медицинске опреме итд. У потпуно различитим областима.

Изговарајући реч "батерија", они значе или саму батерију или батеријску ћелију. Неколико серија или паралелно повезаних једна са другом батеријске ћелије формирају батерију, као и неколико повезаних батерија.
Прва батерија, односно галванска ћелија за вишекратну употребу појавила се, према званичним подацима, 1803. Створио га је немачки физичар и хемичар Јоханн Вилхелм Риттер. Оерстедов пријатељ, Риттер, није био научник, проучавао је хемијски ефекат светлости, спроводио експерименте са електролизом, успут, он припада открићу ултраљубичастог дела електромагнетног спектра.
Док је експериментирао са волтаичном колоном, Риттер је узео педесет кругова бакра, комадиће влажне крпе и сачинио колону од педесет таквих кругова и влажне крпе између њих. Пролазећи струјом из волтаичног стуба кроз структуру, Риттер је установио да му се ступ напуни и да сам постаје извор струје. Ово је била прва батерија.
Реверзибилност хемијске реакције у електролиту и на електродама батерије омогућава вам да вратите радни капацитет батерије - да бисте је напунили након пражњења. Струја током пуњења пролази кроз батерију у супротном смеру од пражњења.
На пример, батерија са оловном киселином ради због електрохемијских реакција олова и оловног диоксида у сумпорној киселини. Формуле у наставку приказују реверзибилне реакције које се дешавају на аноди и на катоди: с лева на десно - реакција током пражњења, са десна на лево - наелектрисање.
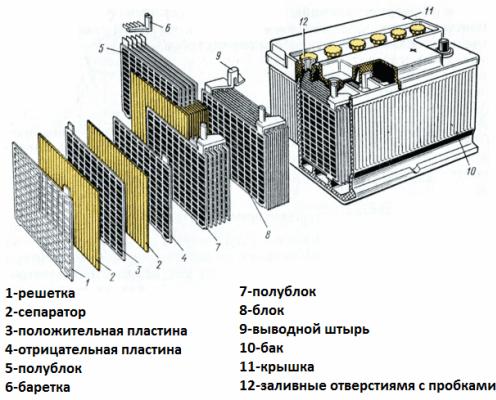
Размотрите сада батеријски уређај као пример батерије за стартовање аутомобила. Напон му је 12 волти. Батерија се састоји од шест ћелија спојених у низу, одвојених преградама.
Серијска веза у овом случају значи да је негативни терминал једне ћелије повезан са позитивним терминалом следеће ћелије.
Сваки елемент укључује пар електрода решетке од легуре олова и антимона уроњене у електролит, који је 38% водени раствор сумпорне киселине. Порозни сепаратор изолише електроде једна од друге, спречавајући кратке спојеве између њих, али слободно пропушта електролит кроз себе. Односно, течност испуњава и ћелије оловних плоча и поре сепаратора.
Истоимене плоче међусобно су повезане оловним скакачима, као и пакети тањура одвојени преградама које чине појединачне елементе, а терминали акумулатора такођер су од олова.
Закључци акумулатора за аутомобиле увек се мало разликују један од другог - позитивни терминал је већег пречника од негативног како не би дошло до грешке приликом повезивања.
Кућиште акумулатора направљено је од диелектричног материјала отпорног на агресивно окружење, температурне екстремне разлике и вибрације. Данас су кућишта за почетне батерије направљена од полипропилена.
Футрола је херметички затворена посуда са поклопцем, опремљена прирубницама за трајно постављање.У кућиштима старих батерија увек су били обезбеђени утикачи за сваку галванску ћелију која чини батерију, тако да се по потреби може додати дестилована вода. Модерни утикачи за батерије без одржавања на кућиштима немају.
Остали чланци о батеријама и њиховој употреби:
Дијаграми повезивања са батеријом
Како су батерије за соларне електране
Погледајте и на електрохомепро.цом
: