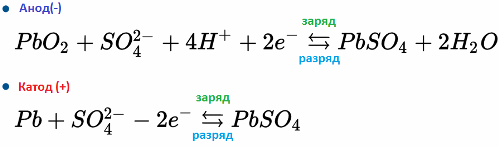Categorías: Como funciona, Electricista de automóviles
Cantidad de vistas: 16526
Comentarios sobre el artículo: 0
El dispositivo y el principio de funcionamiento con batería.
La batería eléctrica se llama fuente de corriente química reutilizable. Los procesos químicos dentro de la batería, en contraste con los de las celdas galvánicas desechables, como las baterías alcalinas o de sal, son reversibles. Los ciclos de carga-descarga, acumulación y retorno de energía eléctrica pueden repetirse muchas veces.
Por lo tanto, el principio de funcionamiento de la batería le permite utilizarla cíclicamente para el suministro de energía autónomo de una variedad de dispositivos, dispositivos portátiles, vehículos, equipos médicos, etc. en áreas completamente diferentes.

Hablando la palabra "batería", significan la batería en sí o la celda de la batería. Varias celdas de batería conectadas entre sí en serie o en paralelo forman una batería, así como varias baterías conectadas.
La primera batería, es decir, una celda galvánica reutilizable, apareció, según cifras oficiales, en 1803. Fue creado por el físico y químico alemán Johann Wilhelm Ritter. Un amigo de Oersted, Ritter, no siendo científico, estudió el efecto químico de la luz, realizó experimentos con electrólisis, por cierto, pertenece al descubrimiento de la parte ultravioleta del espectro electromagnético.
Mientras experimentaba con una columna voltaica, Ritter tomó cincuenta círculos de cobre, piezas de tela húmeda, y formó una columna de cincuenta círculos y tela húmeda entre ellos. Al pasar la corriente de la columna voltaica a través de la estructura, Ritter descubrió que su poste estaba cargado y se convirtió en una fuente de electricidad. Esta fue la primera batería.
La reversibilidad de la reacción química en el electrolito y en los electrodos de la batería le permite restaurar la eficiencia de la batería, cargarla después de la descarga. La corriente durante la carga pasa a través de la batería en la dirección opuesta a la descarga.
Por ejemplo, una batería de plomo-ácido funciona debido a las reacciones electroquímicas de plomo y dióxido de plomo en ácido sulfúrico. Las fórmulas a continuación reflejan reacciones reversibles que ocurren en el ánodo y en el cátodo: de izquierda a derecha - reacción durante la descarga, de derecha a izquierda - carga.
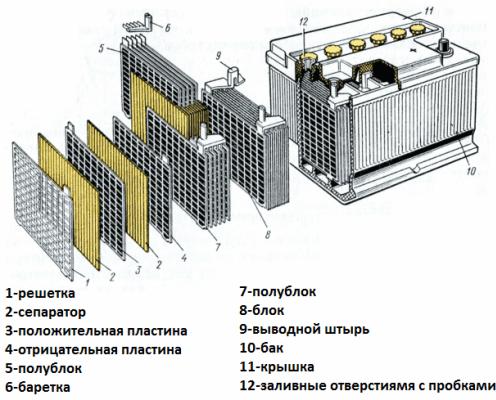
Considere ahora el dispositivo de batería como un ejemplo de una batería de arranque de automóvil. Su voltaje es de 12 voltios. La batería consta de seis celdas conectadas en serie, separadas por particiones.
La conexión en serie en este caso significa que el terminal negativo de una celda está conectado al terminal positivo de la siguiente celda.
Cada elemento incluye un par de electrodos reticulados de una aleación de plomo-antimonio sumergido en un electrolito, que es una solución acuosa de ácido sulfúrico al 38%. El separador poroso aísla los electrodos entre sí, evitando cortocircuitos entre ellos, pero pasa libremente el electrolito a través de sí mismo. Es decir, el líquido llena tanto las celdas de las placas de plomo como los poros de los separadores.
Las placas del mismo nombre están interconectadas por puentes de plomo, así como los paquetes de placas separados por particiones, que forman los elementos individuales, y los terminales de la batería también están hechos de plomo.
Las conclusiones de la batería del automóvil son siempre ligeramente diferentes entre sí: el terminal positivo tiene un diámetro mayor que el negativo para no cometer un error al conectarse.
La caja de la batería está hecha de un material dieléctrico resistente a ambientes agresivos, temperaturas extremas y vibraciones. Hoy, las cajas de batería de arranque están hechas de polipropileno.
La caja es un contenedor herméticamente sellado con tapa, equipado con bridas para un montaje duradero.En los casos de baterías viejas, siempre se han proporcionado enchufes para cada una de las celdas galvánicas que forman la batería, de modo que se pueda agregar agua destilada si es necesario. Los enchufes de batería modernos libres de mantenimiento en los casos no tienen.
Otros artículos sobre baterías y su uso:
Diagramas de conexión de batería
¿Cómo son las baterías para las plantas de energía solar?
¿Cómo se organizan y funcionan los cargadores de batería?
Ver también en bgv.electricianexp.com
: